近年来,中国与非洲国家的关系迅速发展,特别是中国对非洲的投资明显增多,以致起引了某些西方人士的非议,甚至荒唐地认为中国在非洲推行新的“殖民政策”。
结合材料,从主权国家的角度,驳斥“中国在非洲推行新的‘殖民政策”’这一言论。
相关问题推荐
-
T℃时,将3molA和1molB气体通入体积为2L的密闭容器(体积不变),发生反应:
3A(g)+B(g)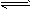 xC(g)。2min后达平衡,剩余0.8molB,C的浓度为0.4mol/L。
xC(g)。2min后达平衡,剩余0.8molB,C的浓度为0.4mol/L。
(1)x=______;
(2)若向平衡混合物中通入少量He,则平衡_____(填“正向移动”、“逆向移动”或“不移动”)
(3)若向平衡混合物中再充入amol C,在T℃时达新平衡,此时B的物质的量为______(用含a的式子表示):
(4)若上述反应在相同温度和容器中进行,欲使反应达平衡时c的物质的量分数与原平衡相等,则起始加入三种物质的量n (A)、n (B)、n (C)间应满足的关系式为______。 -
在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1gN2和1gH2,乙容器中充入2gN2和2gH2。下列叙述中,错误的是
[ ]
A.化学反应速率:乙>甲B.平衡后N2的浓度:乙>甲C.H2的转化率:乙>甲D.平衡混合气中H2的体积分数:乙>甲
-
已知工业制氢气的反应为CO(g)+H2O(g)
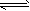 CO2(g)+H2(g),反应过程中能量变化如图所示。在500 ℃时的平衡常数K=9。若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态。
CO2(g)+H2(g),反应过程中能量变化如图所示。在500 ℃时的平衡常数K=9。若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态。 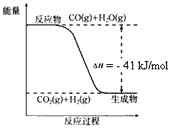
(1)增加H2O(g)的浓度,CO的转化率将_____(填“增大”“减小”或“不变”)。 (2)平衡常数的表达式K=___\_。400℃时的平衡常数K_______9(填“>”“<”或”“=”)。 (3)500℃时,10min内v(H2O)=___\__,在此过程中体系的能量将____\_(填“增加”或“减少”)________kJ。 (4)已知2H2(g) + O2(g) = 2H2O(g) ΔH=-484kJ/mol 结合上图写出CO完全燃烧生成CO2的热化学方程式:___________。
-
定条件下,存在可逆反应X(g)+2Y(g)
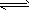 3Z(g),若X、Y、Z起始浓度分别为
3Z(g),若X、Y、Z起始浓度分别为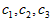 (均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.2mol/L,0.06mol/L,则下列判断不合理的是
(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.2mol/L,0.06mol/L,则下列判断不合理的是[ ]
A.
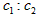 =l:2B.达平衡状态时,生成Z的速率是生成X速率的3倍C.X、Y的转化率不相等D.C2的取值范围为
=l:2B.达平衡状态时,生成Z的速率是生成X速率的3倍C.X、Y的转化率不相等D.C2的取值范围为
-
恒温、恒压下,在一可变容器下反应,A(g) + B(g)
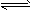 C(g)
C(g)
(1)开始时,放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的量为_________mol
(2)若开始时放入3mol
A、3molB,到达平衡后生成C的物质的量为______mol
(3)若开始时,放入Xmol
A、2molB和1molC,到达平衡后,A和C的物质的量分别是Ymol和3amol,
则X=___\_,Y=____
(4)若在(3)的平衡状态上再加入3molC,待再次平衡后,C的物质的量分数是____
