材料一:2003~2007年我国粮食总产量及其增长速度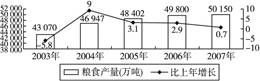 注:①2008年我国粮食供求关系出现转折性变化,正由过去的供求总量基本平衡,向供求总量偏紧、品种结构矛盾日益突出转变。②据联合国相关机构统计,国际粮价自2002年开始上涨,到今年初已累计上涨65%。资料显示:2007年前三季度我国全国粮食生产价格比去年同期上涨7.7%。预测2008年我国粮食市场价格有可能保持在高位运行基础上的基本稳定。材料二:2006年我国及广东省耕地面积统计
注:①2008年我国粮食供求关系出现转折性变化,正由过去的供求总量基本平衡,向供求总量偏紧、品种结构矛盾日益突出转变。②据联合国相关机构统计,国际粮价自2002年开始上涨,到今年初已累计上涨65%。资料显示:2007年前三季度我国全国粮食生产价格比去年同期上涨7.7%。预测2008年我国粮食市场价格有可能保持在高位运行基础上的基本稳定。材料二:2006年我国及广东省耕地面积统计

耕地面积(万亩)
人均耕地面积(亩)
全国
182700
1.39
广东
3719.3
0.4注:①联合国粮农组织划定的警戒线为人均耕地面积0.8亩。
②2001~2005年间,广东省共减少耕地258.45万亩,平均每年减少51.69万亩,粮食自给率不足40%。材料三:党的十七届三中全会审议通过《中共中央关于推进农村改革发展若干重大问题的决定》。《决定》指出:坚持改革开放,必须把握农村改革这个重点,在统筹城乡改革上取得重大突破,给农村发展注入新的动力,为整个经济社会发展增添新的活力。推动科学发展,必须加强农业发展这个基础,确保国家粮食安全和主要农产品有效供给,促进农业增产、农民增收、农村繁荣,为经济社会全面协调可持续发展提供有力支撑。请回答下列问题:(1)材料一、材料二各反映了什么经济现象?(5分)(2)材料一、二和材料三之间有何内在联系?为什么?(4分)(3)针对材料中反映出来的问题,为维护国家粮食安全,请你为我国政府提几点建议。(8分)
相关问题推荐
-
高三(10)班同学成立了探究性学习小组,对我国财税的有关情况进行调查研究。(1)通过努力,同学们搜集到下列资料。图 “十五”期间我国税收总额(亿元)
 表 “十五”期间,我国东、中、西部地区税收收入占全国税收收入总额的比重
表 “十五”期间,我国东、中、西部地区税收收入占全国税收收入总额的比重地区
东部
中部
西部
占全国税收收入总额的比重
70.8%
15.5%
13.7%
比“九五”期间增速
20.1%
18.3%
17.9%请你说出搜集资料的主要途径。(4分)
(2)同学们在调查研究中发现了这一现象:我省某县政府给该县机械厂厂长张某奖励30万元,并明确宣布此奖免缴个人所得税。理由是他超额完成承包利税指标,对本县的经济发展作出了突出贡献。请你说明该县政府重奖“纳税大户”的做法是否正确。为什么?(6分)(3)同学们在调查研究过程中发现,有意偷逃税款现象在现实生活中较为普遍,有些人对这一现象还无动于衷。偷逃税款对我国经济社会生活会产生什么影响?你认为应采取哪些措施来克服偷逃税款现象?(10分)
-
X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y
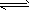 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于[ ]
A.33% B.40% C.50% D.65%
-
在mA(g) + nB(g)
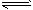 pC(g) + qD(g)的反应中,(m、n、p、q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为
pC(g) + qD(g)的反应中,(m、n、p、q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为 [ ]
A.2 :3 :2 :3 B.2 :2 :3 :3 C.3 :1 :2 :2 D.3 :1 :2 :3
-
在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g)
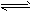 3C(g),已知加入1 molA和3molB且达到平衡后,生成了amol C。
3C(g),已知加入1 molA和3molB且达到平衡后,生成了amol C。
(1)达到平衡时,C在反应混合气体中物质的量分数为_______(用字母a表示)。
(2)在相同实验条件下,若在同一容器中改为加入2molA和6molB,达到平衡后,C的物质的量为
___\_mol(用字母a表示)。此时C在反应混合气体中物质的量的分数_________。(填“增大”、“减小”或“不变”)
(3)在相同实验条件下,若在同一容器中改为加入2molA和8molB,若要求平衡后C在反应混合气体中体积分数不变,则还应加入C_________mol。 -
在一定温度下,向一个5L的密闭容器中,通入2 mol N2和8 mol H2及固体催化剂,使之反应。已知:
N2(g)+3H2(g)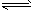 2NH3(g) ΔH=-92.2 kJ·mol-1。平衡时容器内气体压强为起始时的80%。
2NH3(g) ΔH=-92.2 kJ·mol-1。平衡时容器内气体压强为起始时的80%。
(1)计算平衡时容器内NH3的体积分数为___\_,该该温度下该反应的平衡常数为:______。(利用三段式计算,要有过程)
(2)加入2 mol N2和8 mol H2,达到平衡时,放出热量为________(填序号)。
A.大于92.2 kJ B.等于92.2 kJ C.小于92.2 kJ D.可能大于或小于或等于92.2 kJ
(3)在相同容器中,降低温度,通入2 mol NH3和1 mol H2及固体催化剂,反应达到平衡时NH3的体积分数是否为1/4,下列判断正确的是________(填序号)。
A.一定等于1/4 B.一定大于1/4 C.一定小于1/4 D.可能大于或小于或等于1/4
