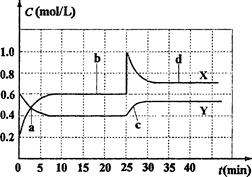
A.图中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C.反应进行至25min时,曲线发生变化的原因是加入0.4molN2O4
D.若要达到与d相同的状态,在25min时还能采取的措施是适当缩小容器体积
相关问题推荐
-
已知:N2(g)+3H2(g)
 2NH3(g);ΔH="-92.4"kJ·mol-1。请回答:
2NH3(g);ΔH="-92.4"kJ·mol-1。请回答:
(1)合成氨工业中采取的下列措施可以用勒夏特列原理解释的是 (填字母)。
a.用铁触媒加快化学反应速率 b.采用较高压强(20MPa~50MPa)
c.将原料气中的少量CO等气体净化除去d.将生成的氨液化并及时从体系中分离出来
(2)一定温度下,在密闭容器中充入1molN2和3molH2并发生反应。若容器容积恒定,达到平衡时,气体的压强为原来的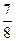 ,则N2的转化率a1= ,此时,反应放热 kJ;
,则N2的转化率a1= ,此时,反应放热 kJ; -
在120 ℃时分别进行如下四个反应:
A.2H2S+O2====2H2O+2S↓
B.2H2S+3O2====2H2O+2SO2
C.C2H4+3O2=====2H2O+2CO2
D.C4H8+6O2====4H2O+4CO2 (1)当反应在容积固定的容器内进行,反应前后气体密度(d)的气体总压强(p)分别符合关系式d
前=d后和p前>p后的是____;符合关系式d前=d后和p前=p后的是______。(请填写反应的代号) (2)若反应在压强恒定容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前
-
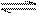 X(g)+Y(g) Z(g)+W(s);△H<0下列叙述正确的是 ( )
X(g)+Y(g) Z(g)+W(s);△H<0下列叙述正确的是 ( )A.增加少量W,正反应速率减小
B.当容器中气体的密度不变时,反应达到平衡
C.降低温度,平衡不移动
D.平衡后加入Z,则W的质量增大
-
A.O2的消耗速率等于NO的消耗速率
B.容器中存在N2,O2,NO三种气体
C.容器内混合物总的物质的量不随时间而改变
D.单位时间内每生成nmolN2的同时生成2nmolNO
-
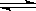
A.起始反应时,甲容器的正反应速率与乙反应的正反应速率相同
B.均达到平衡后,反应速率乙容器是甲容器的2倍
C.均达到平衡后,混合气体的平均相对分子质量乙容器是甲容器的2倍
D.均达到平衡后,再向乙容器加2mol
A、2molB,达到新的平衡后,C的体积分数乙容器大于甲容器
