阅读下列资料,完成下列要求:(18分)
我国有相当一部分耕地质量低,农作物生长不良,成为农业低产区。图为“我国某农业低产区的分布地区示意图”。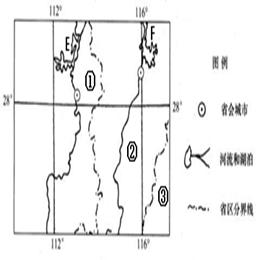
(1)E湖泊近百年来面积不断在缩小,分析其缩小的原因(4分)
(2)图示地区为我国主要的农业低产区,结合所学知识简述其主要成因。(4分)
(3)简述图示地区的自然地理特征(10分)
相关问题推荐
-
恒温(1100℃)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g)→Na2S(s)+4H2O(g)。下列说法正确的是()
A.该反应的平衡常数表达式_K_=_c_(H2O)/_c_(H2)
B.若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态
C.若Na2SO4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变
D.若初始时投入2.84gNa2SO4与一定量H2,反应达平衡时容器内固体共有2.264g,则Na2SO4的转化率为45%
-
在容积可变的密闭容器中,2mol
 和8mol
和8mol 在一定条件下反应,达到平衡时,
在一定条件下反应,达到平衡时, 的转化率为25%,则平衡时氨气的体积分数接近于
的转化率为25%,则平衡时氨气的体积分数接近于A.5%
B.10%
C.15%
D.20%
-
工业废水中常含有一定量的
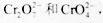 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
其中第①步存在平衡:
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr O
O
 和CrO
和CrO 的浓度相同
的浓度相同
b.2v (Cr O
O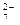 ) ="v" (CrO
) ="v" (CrO )
)
c.溶液的颜色不变
(3)第②步中,还原1mol Cr O
O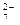 离子,需要 mol的FeSO
离子,需要 mol的FeSO ·7H
·7H O。
O。
(4)第③步生成的Cr(OH) 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡: 
常温下,Cr(OH) 的溶度积
的溶度积 ,要使c(Cr3+)降至10
,要使c(Cr3+)降至10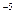 mol/L,溶液的pH应调至 。
mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr O
O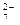 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH) 沉淀。
沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。 -
恒压密闭容器中充入2 mol X和5 mol Y,发生反应:X(g)+3Y(g)
 2Z(g),温度分别为T1和T2时,X的转化率α(X) 随时间变化的关系如图。下列结论正确的是
2Z(g),温度分别为T1和T2时,X的转化率α(X) 随时间变化的关系如图。下列结论正确的是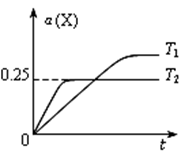
A.该反应正反应吸热
B.达到平衡后,其它条件不变,通入稀有气体,平衡向正反应方向移动
C.达到平衡后,其它条件不变,降低温度,正逆反应速率均减小,Z的体积分数也减小
D.在T2℃时,若开始加入1molX、3molY和2molZ,达到平衡后α(X)>0.25
-
一定条件下,在一定体积的恒容密闭容器中,CO2与NH3在一定条件下反应生成尿素 CO2(g)+2NH3(g)
 CO(NH2)2(s)+H2O(g) 根据题意完成下列各题;
CO(NH2)2(s)+H2O(g) 根据题意完成下列各题;  (1)500℃,用尿素表示该反应的反应速率,v(尿素)= mol/min. (2)该反应的正反应△H 0(填“>”或“<”)。 (3)上图2表示某温度时一些反应物与产物物质的量(n)随时间(t)变化的关系。 ①对于该反应达到平衡状态的判断,下列说法正确的是 。
(1)500℃,用尿素表示该反应的反应速率,v(尿素)= mol/min. (2)该反应的正反应△H 0(填“>”或“<”)。 (3)上图2表示某温度时一些反应物与产物物质的量(n)随时间(t)变化的关系。 ①对于该反应达到平衡状态的判断,下列说法正确的是 。A.混合气体的密度不再发生改变
B.图2中C点时,该反应达到了平衡状态
C.混合气体的压强不再发生改变
D.当消耗了2n mol NH3时,同时生成了n molH2O②反应速率v(CO
2):图中点a b(填“>”、“<”或“=”)。 (4)用该原理生产尿素,工业上一般在220大气压下进行。其它条件不变,与常压相比,220大气压时NH3的转化率 (填增大、减小或不变。)反应的平衡常数K (填增大、减小或不变)。
