问题详情
有一块合金,由三种成分组成,其中一种可用来制照明弹.将此合金进行如下处理: (1)将合金放入热的氢氧化钠溶液中,合金部分溶解并产生气体.过滤,得到溶液A,不溶物B; (2)向A中加入适量盐酸,有白色沉淀生成,继续加入盐酸,白色沉淀减少但不完全消失,过滤得到溶液C,不溶物D; (3)向C中加入过量氨水,有白色沉淀E生成,E不溶于氨水,但能溶于烧碱溶液; (4)B可溶于盐酸,生成溶液F,并放出无色气体,向F中加入氨水,生成白色沉淀G,G不溶于氨水,也不溶于烧碱溶液. 根椐以上事实,判断此合金的三种成分是什么?
A、B、C、D、E、F、G各是什么物质?
未找到的试题在搜索页框底部可快速提交,在会员中心"提交的题"查看可解决状态。
收藏该题
查看答案
相关问题推荐
-
H2CO3、H2PO4、H2SO4、H2SiO4四种含氧酸中酸性最强的是____酸性最弱的是____.
-
元素X、Y和Z都位于短周期,它们的原子序数之和为37,X-和Y+具有相同的电子层结构并能生成离子化合物,则Y位于周期表中第____族;X的原子结构示意图为____;Z与氢元素形成的化合物的电子式为____.
-
原子序数为16的某元素,应在周期表中的第____周期,第____族,其阴离子的化学式是____.
-
氯水中存在如下平衡:
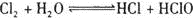 向氯水中加入少量CaCO3,平衡向____移动;向氯水中加入少量NaOH溶液,平衡向____移动.
向氯水中加入少量CaCO3,平衡向____移动;向氯水中加入少量NaOH溶液,平衡向____移动. -
将物质的量浓度和体积都相同的盐酸、Na2CO3溶液、CH3COOH溶液混合并加热,充分反应后,所得溶液的pH____(选填大于、小于或等于)7.
