将1molI2(g)和2molH2置于某2L密闭容器中,在一定温度下发生反应: I2(g)+H2(g)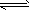 2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线(II)所示:(提示:同条件体积分数=物质的量分数)
2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线(II)所示:(提示:同条件体积分数=物质的量分数)
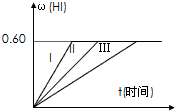
(1)达平衡时,I2(g)的物质的量浓度为________。 (2)若改变反应条件下,在甲条件下ω(HI)的变化如图曲线(I)所示,在乙条件下ω(HI)的变化如图曲线(III)所示。则甲条件可能是________(填入下列条件的序号。下同),乙条件可能是 ________。 ① 恒容条件下,升高温度;② 恒容条件下,降低温度;③ 恒温条件下,缩小反应容器体积; ④ 恒温条件下,扩大反应容器体积;⑤ 恒温恒容条件下,加入适当催化剂。 (3)若保持温度不变,在另一相同的2L密闭容器中加入amol I2(g)、bmol H2和cmol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是:________。
相关问题推荐
-
将2molA和1molB混合装入容积可变的密闭容器中,发生反应:2A(s)+bB(g)
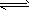 cC(g)达到化学平衡后,C的物质的量浓度为amol·L-1。若在温度一定的条件下,将密闭容器容积变为原来的1/2后,C的物质的量浓度为2amol·L-1,且始终不变。则b、c关系是
cC(g)达到化学平衡后,C的物质的量浓度为amol·L-1。若在温度一定的条件下,将密闭容器容积变为原来的1/2后,C的物质的量浓度为2amol·L-1,且始终不变。则b、c关系是[ ]
A.b+2=c B.b=c C.b+2>c D.b
-
下列省区轮廓与其对应的简称错误的是
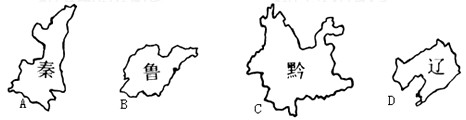
[ ]
A、AB、BC、CD、D
-
在密闭容器中,对于反应2SO2(g) + O2(g)
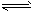 2SO3(g),SO2和O2起始时分别为20mol和10mol,达到平衡时,SO2的转化率为80%,若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率为
2SO3(g),SO2和O2起始时分别为20mol和10mol,达到平衡时,SO2的转化率为80%,若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率为 [ ]
A.10mol和10% B.20mol和20% C.20mol和40% D.30mol和80%
-
在容积为2L的密闭容器中,有反应: mA(g)+nB(g)
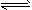 pC(g)+qD(g),经过5分钟达到平衡,此时各物质的变化为:A减少amol/L,C增加2a/3mol/L,B的平均反应速率VB=a/15mol/(L·min),这时若增加体系压强,发现A与C的百分含量不变,则m:n:p:q为
pC(g)+qD(g),经过5分钟达到平衡,此时各物质的变化为:A减少amol/L,C增加2a/3mol/L,B的平均反应速率VB=a/15mol/(L·min),这时若增加体系压强,发现A与C的百分含量不变,则m:n:p:q为 [ ]
A.3:1:2:2 B.1:3:2:2 C.1:3:2:1 D.1:1:1:1
-
2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应: PCl3(g)+Cl2(g)
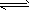 PCl5(g)达平衡时,PCl5为0.40mol,如果此时再充入1.0mol PCl3和 0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g)达平衡时,PCl5为0.40mol,如果此时再充入1.0mol PCl3和 0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是[ ]
A.0.40mol B.0.60mol C.大于0.60mol D.大于0.40mol,小于0.60mol
