已知2SO2(g)+O2(g)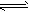 2SO3(g) △H=-196kJ·mol-1, 500℃时将2mol SO2和1molO2装入一体积恒定的 10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:
2SO3(g) △H=-196kJ·mol-1, 500℃时将2mol SO2和1molO2装入一体积恒定的 10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:
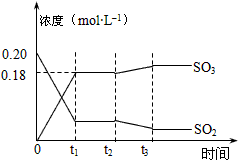
请回答下列问题 (1)用O2表示2分钟内该反应的平均反应速率为________mol·L-1·min-1。计算500℃时该反应的平衡常数 K=________, (2)上图表示该反应在时刻t1达到平衡后,求平衡时O2的转化率___\_,时刻t2因改变某个条件而发生变化的情况:图中时刻t2发生改变的条件可能是__________(写一个即可)。 (3)在上述条件下起始装入的SO2和O2各2mol,达平衡后设SO3的转化率为x,列出求x的方程 ________。(不必求出x) (4)某温度时,该反应的平衡常数K=800,则该温度________500℃(填“>”、“<”、“=”)。
相关标签: 转化率
相关问题推荐
-
某一反应在一定条件下的平衡转化率为25.3%,当有一催化剂存在时,其转化率是()。
A.>25.3%
B.=25.3%
C.
D.接近100%
-
对于循环系统,下列说法不正确的是()。
A、总转化率>单程转化率,总收率>单程收率
B、总转化率=单程转化率,总收率=单程收率
C、总转化率>单程转化率,总收率<单程收率
D、总转化率<单程转化率,总收率>单程收率
-
物质的量之比为2∶3的N2和H2,在一定条件下反应,并达到平衡。在此过程中,下列说法正确的是( )
A.在建立平衡的过程中,N2和H2的物质的量之比始终是2∶3
B.N2的转化率始终为H2转化率的2倍
C.N2的转化率始终为H2转化率的1/2
D.达到平衡时,平衡体系的总物质的量与起始时的总物质的量之比可为1∶2
-
太阳能电池已为人们所熟悉。现在的太阳能电池,其能量转化率在10%左右,因而用途有限。如果想获得较大的电功率,就需要昂贵的投资、巨大的装置,占用巨大的面积或空间,这实际上是不可行的。因此唯有在提高其能量转化率上下工夫,以拓展其应用范围。以下哪项,从上述题干中推出最为恰当?
A.太阳能电池的能量转化率越高,其所需面积就越小。
B.太阳能电池面积越大,其能量转化率就越高。
C.太阳能电池的能量转化率越高,获得的电功率就越大。
D.缺乏投资是太阳能电池难以得到广泛应用的原因。 -
某一反应在一定条件下的平衡转化率为25.3%,当有一催化剂存在时,其转化率为()。
A、>25.3%
B、不变
C、<25.3%
D、接近100%
