问题详情
反应CO(g)+H2O(g)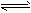 CO2(g)+H2(g)ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表
CO2(g)+H2(g)ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表

此时反应中正、逆反应速率的关系式是
[ ]
A.v(正)>v(逆)B.v(正)<v(逆)C.v(正)=v(逆)D.无法判断
相关标签: 逆反应 化学平衡 关系式
未找到的试题在搜索页框底部可快速提交,在会员中心"提交的题"查看可解决状态。
收藏该题
查看答案
相关问题推荐
-
将等物质的量的X.Y气体充入一容积可变的密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)+2M(s)
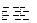 2Z(g);
2Z(g);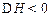 。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )
。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )改变的条件
正.逆反应速率变化
新平衡与原平衡比较
A
升高温度
逆反应速率增大量大于正反应速率增大量
X的体积分数增大
B
增大压强
正反应速率增大,逆反应速率减小
Z的浓度不变
C
减小压强
正.逆反应速率都减小
Y的体积分数变大
D
充入一定量的Z
逆反应速率增大
X的体积分数变大
-
25℃时,反应的,若升高温度,()。
A、正反应速率增大,逆反应速率减小
B、正反应速率减小,逆反应速率增大
C、正反应速率增大,逆反应速率增大
D、正反应速率减小,逆反应速率减小
-
下列哪种表述化学平衡常数的特性是错误的()
A、化学平衡常数与反应物的最初浓度无关
B、化学平衡常数与平衡状态时生成物的最初浓度无关
C、温度可改变化学平衡常数
D、对于有固体物质参加的多相可逆反应,化学上规定纯固体的浓度等于1
-
对于化学可逆反应,催化剂能同时降低正逆反应的活化能,使正逆反应加速,但不能使化学平衡发生移动。
A、对
B、错
